本文解读发表于PNAS的重磅研究,该研究提出结构感知型深度学习框架 DeepDegradome,将片段药物发现、分子对接与生成式人工智能深度融合,构建了不依赖已知配体的全流程药物设计体系。该平台可直接依据靶标蛋白结构,全自动生成高亲和力小分子配体与高效 PROTAC 降解剂,在 WDR5、CDK9 等传统方法难以攻克的靶点上取得突破性实验验证,为 “不可成药” 靶点的药物研发提供了自动化、高通量的全新解决方案。

在现代药物研发领域,PROTAC(靶向蛋白降解嵌合体) 凭借独特的作用机制,成为颠覆传统小分子疗法的前沿技术。与仅能抑制蛋白功能的常规药物不同,PROTAC 可以利用细胞自身的泛素化 - 蛋白酶体系统,将致病蛋白直接清除,因此对传统小分子难以干预的靶点具有巨大应用潜力。
然而 PROTAC 的研发长期存在难以突破的瓶颈。传统设计思路必须先找到可结合靶标的弹头配体,再将其与 E3 连接酶配体通过连接链拼接,整个研发过程高度依赖已有的分子骨架。对于大量缺乏已知配体的靶点,PROTAC 技术几乎无法应用,这也让众多关键致病蛋白长期处于 “不可成药” 状态。
近期发表在PNAS的一项研究彻底打破了这一限制,研究团队开发出DeepDegradome平台,成为全球首个能够直接从蛋白结构一体化生成小分子配体与 PROTAC 分子的人工智能系统。该平台不需要预设片段、不需要依赖已知配体、不需要人工指定连接位点,仅输入蛋白三维结构,就能自动生成具有高活性的小分子与可有效降解靶标的 PROTAC 分子。这一成果标志着 AI 药物研发真正实现了从 “0 到 1” 的原创分子生成。
一、传统 PROTAC 研发面临的核心困境
PROTAC 分子由靶标配体、E3 连接酶配体与连接链三部分组成。尽管其作用机制清晰,但在实际研发中,传统模式长期面临三大难以突破的困境。
现有的 PROTAC 研发高度依赖已知弹头配体,而大量与肿瘤、神经退行性疾病相关的关键蛋白,结构平坦、缺乏明确结合口袋,长期无法获得可用的小分子配体,直接导致 PROTAC 设计无法开展。
在配体受限的前提下,现有研发方法只能在有限范围内优化连接链,无法对弹头与 E3 配体进行同步创新,导致化学空间探索严重不足,难以获得活性与成药性兼具的理想分子。
多数计算模型与生成式 AI 仅基于字符串或二维结构进行生成,忽略蛋白口袋的三维空间环境,导致大量生成的分子无法与靶标有效结合,实际有效率极低,后续实验筛选成本高、周期长、成功率低。
这些问题共同导致 PROTAC 这种极具潜力的技术,长期难以覆盖真正具有临床价值的难成药靶点。
二、AI 突破:DeepDegradome 一体化从头设计体系
DeepDegradome 的核心突破,在于构建了从片段筛选到配体生成,再到 PROTAC 设计的全自动、端到端设计体系,实现了真正意义上的从头药物设计。
平台首先构建覆盖广泛药物优势结构的高质量片段库,通过自研的 iFitDock 对接算法,在不依赖任何已知信息的前提下,精准识别片段在蛋白口袋中的结合模式与关键作用位点。
在片段结合信息的基础上,系统通过智能连接与片段生长策略,将低亲和力片段逐步组装为具有高亲和力、类药性质的完整小分子,全程不需要人工干预,也不依赖任何已有的配体模板。
在获得优质配体后,平台进一步基于靶标蛋白与 E3 连接酶的界面特征,自动设计长度、柔性、构象均最优的连接链,同步保证三元复合物稳定性与降解活性,最终生成具备高效降解能力的 PROTAC 分子。
这一完整流程让 DeepDegradome 可以直接从蛋白结构出发,完成过去需要数年时间才能实现的药物分子设计工作。
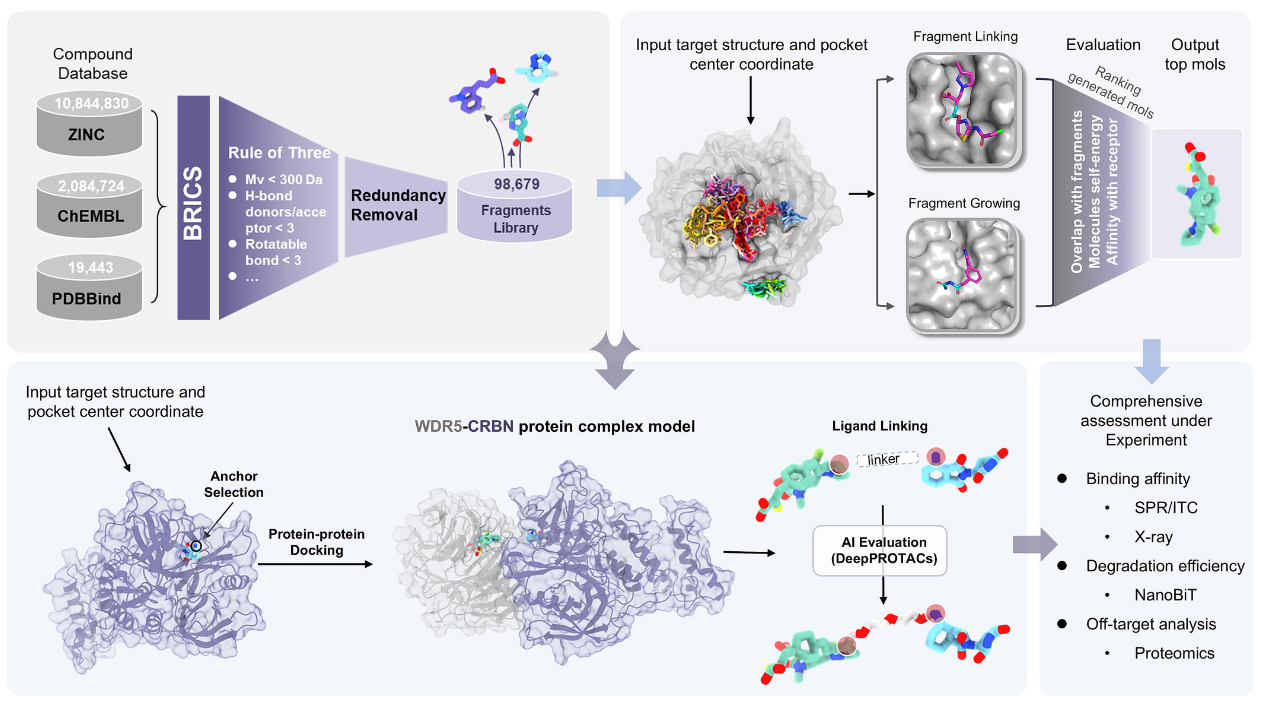
图1 DeepDegradome 一体化配体与 PROTAC 从头设计框架
2.1 结构感知的片段智能组装技术
DeepDegradome 并非简单的片段拼接,而是以蛋白口袋三维结构与药效特征为约束的精准生成。
平台首先将蛋白结合口袋划分为多个子区域,识别出对结合贡献最大的热点区域与关键残基。在此基础上,系统自动生成包含疏水、氢键、电荷等约束的三维药效团模型,让分子生成始终与靶点结构高度匹配。
在药效团引导下,片段以合理的空间构象进行连接与生长,确保生成的分子能够完美契合口袋形状,同时保持合理的分子张力与结合能。这种结构感知的生成模式,从源头大幅降低无效分子比例,显著提升可用分子产出率。
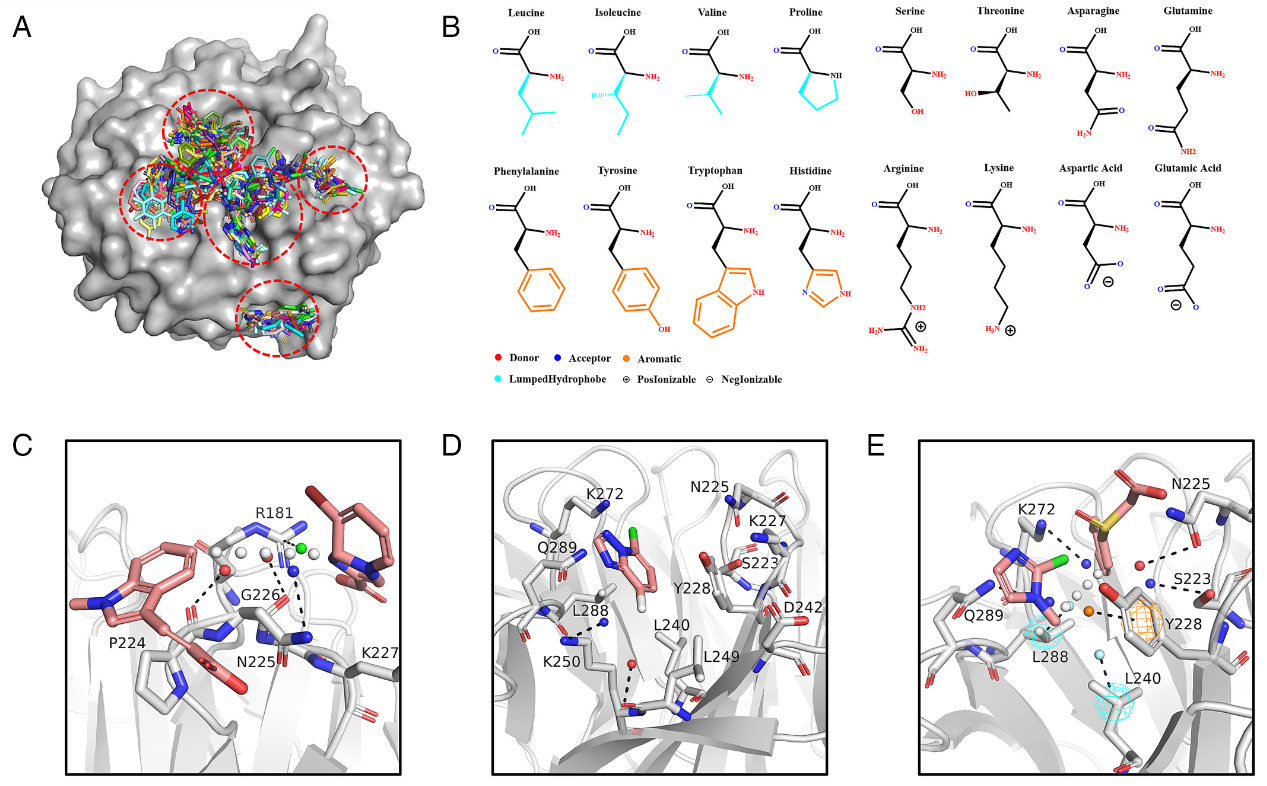
图2 基于蛋白口袋的片段筛选与三维药效团配体生成
2.2 面向三元复合物的 PROTAC 智能优化
决定 PROTAC 活性的核心并非单独的配体亲和力,而是靶标 - PROTAC - E3 三元复合物的稳定性。DeepDegradome 是全球少数将三元复合物界面纳入生成约束的 AI 平台。
系统先通过蛋白 - 蛋白对接预测靶标与 E3 连接酶的相互作用界面,再根据界面距离、电荷分布、空间位阻等特征,自动优化连接链的长度、柔性与连接位点,使最终生成的 PROTAC 分子能够高效拉近靶标与 E3,促进泛素化转移。
平台还搭载深度学习预测模型,直接对生成的 PROTAC 进行降解活性打分,优先选择 DC50 低、Dmax 高的潜在高效分子,大幅减少实验验证成本。
三、实验验证:在难成药靶点上实现突破性活性
研究团队在多个靶点上对 DeepDegradome 进行系统评测,结果显示其在生成成功率、结合亲和力、类药性等指标上全面超越现有主流模型。在 20 个代表性靶点的测试中,分子生成成功率达到 92.2%,生成分子的键长、键角分布与上市药物高度一致,合成可行性与成药性均满足药物研发要求。
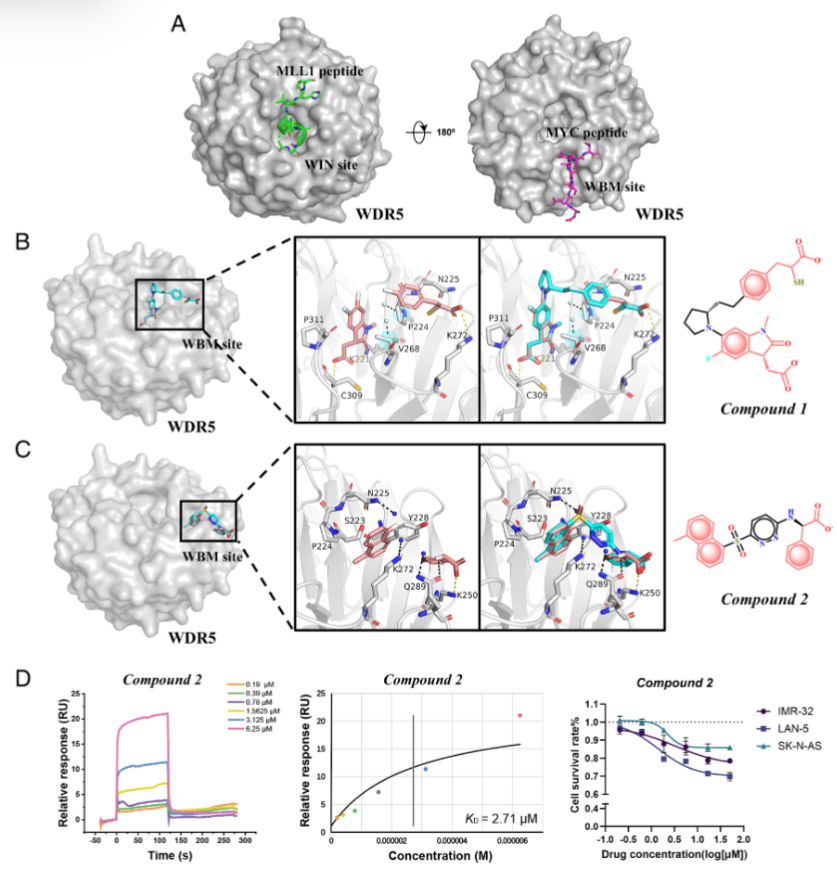 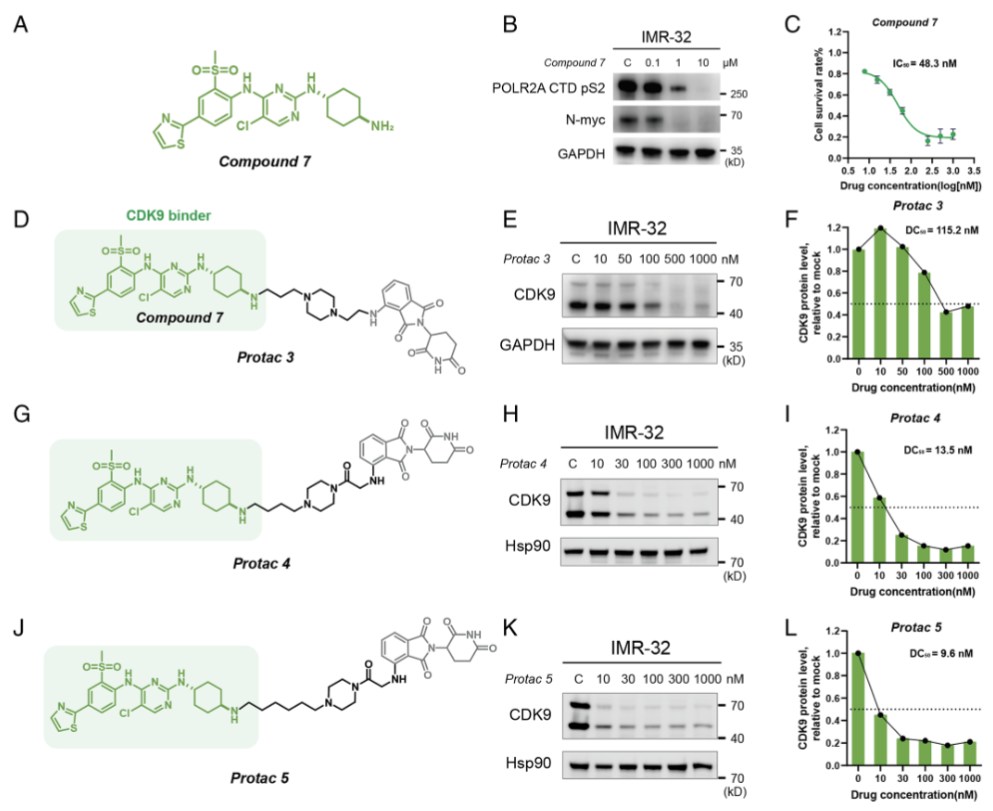 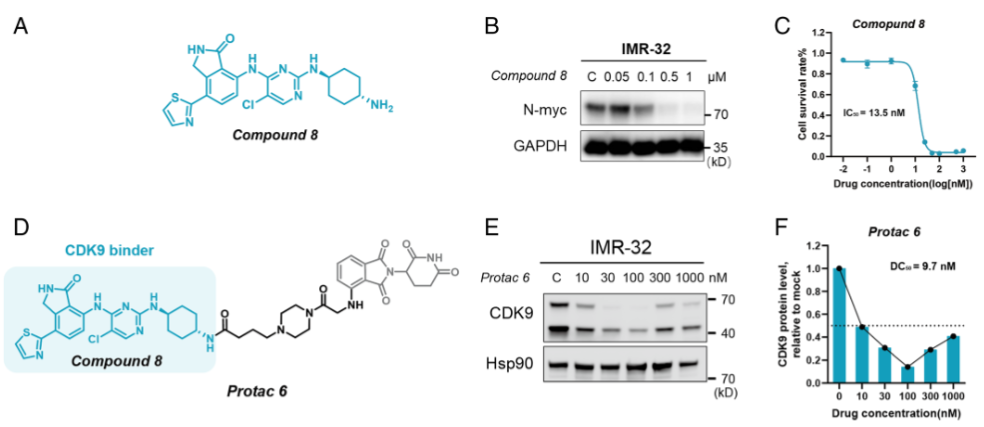
图3 难靶 WDR5 与 CDK9 的 AI 生成分子活性验证
3.1 WDR5 靶点:攻克平坦口袋 “不可成药” 难题
WDR5 是调控 MYC 通路的关键蛋白,与多种恶性肿瘤高度相关,但因其表面平坦、缺乏明显口袋,长期被视为典型难成药靶点。
DeepDegradome 在不使用任何已知配体的前提下,直接从头生成全新骨架小分子,实验验证显示亲和力达到 2.71 μM,并且能够在细胞内有效抑制 WDR5 与 MYC 的相互作用,抑制肿瘤细胞增殖。解析的复合物晶体结构显示,AI 预测的结合模式与实验结果几乎完全一致,证明了平台的高精度预测能力。
基于从头生成的配体,平台进一步设计出可有效降解 WDR5 的 PROTAC 分子,实现浓度依赖性的靶标清除,为该靶点的药物开发提供全新路径。
3.2 CDK9 靶点:纳米级高活性抑制剂与 PROTAC
在 CDK9 这一经典转录调控激酶靶点上,DeepDegradome 展现出更强的生成能力。AI 从头设计的小分子配体在细胞水平实现 13.5 nM 的高活性,可显著下调 MYC 表达并抑制 Pol Ⅱ 磷酸化。
进一步生成的 CDK9 PROTAC 分子表现更加强劲,DC50 最低可达 9.6 nM,最大降解率 Dmax 达到 88%,同时在肿瘤细胞增殖抑制实验中 IC50 达到 4.28 nM,活性远超大量已报道分子。
所有生成的分子均为全新骨架,与已知配体结构相似度低,证明平台具备原创性新药分子研发能力。
四、科学与产业意义:开启 AI 驱动的自动化药物研发时代
DeepDegradome 的突破不仅是算法与工具的进步,更是小分子与 PROTAC 药物研发范式的革新。
它首次实现不依赖已知配体、直接从蛋白结构生成高活性原创小分子,为大量缺乏配体的 “孤儿靶点” 提供了可行的研发路径。它首次实现配体生成、连接链设计、三元复合物优化全流程自动化,将传统药物发现的时间成本从数年缩短至数月甚至数周。它以结构感知的方式进行生成,大幅降低实验筛选成本与失败率,让 PROTAC 技术可以真正普惠更多靶点与疾病领域。
对于生物医药产业而言,这一平台可以显著提升研发效率、降低研发成本、加速临床前候选化合物的产出,尤其对攻克传统手段无法应对的难成药靶点具有不可替代的价值。
五、总结
DeepDegradome 建立了一套从蛋白结构到高活性小分子,再到高效 PROTAC 降解剂的全流程人工智能设计体系。它不依赖已知配体、不局限于现有骨架、不依赖人工经验,仅依靠靶点结构就能自动生成具有高活性的原创药物分子。
在 WDR5 与 CDK9 等关键靶点上的实验验证表明,该平台能够稳定生成高亲和力小分子与强效 PROTAC,预测精度与实验结果高度一致。
这项研究标志着AI 药物研发正式进入原创分子从头设计时代。未来,小分子与 PROTAC 药物研发将不再高度依赖经验与运气,而是转变为精准、可预测、高通量的自动化工程,为攻克更多疑难疾病提供前所未有的工具支持。
论文链接:https://doi.org/10.1073/pnas.2518248123
| 


























