本文解读 2026 年发表于Science的重磅综述《 Reimagining human-centric drug development with new approach methodologies 》,系统阐述新型方法学(NAMs)如何以人类源细胞体系、类器官、器官芯片和人工智能计算模型为核心,构建更贴合人体生理的药物研发体系。文章梳理了传统动物实验模式的固有局限与全球监管变革,解析了人源细胞模型、微生理系统与智能计算三大技术支柱,展示了 NAMs 在靶点发现、安全性评价、临床预测与个体化医疗中的突破性应用,并明确指出行业未来走向:未来药研多步相关的动物实验验证将逐步取消,而是以人源细胞系构建的类器官、器官芯片和计算模型的结果为重要依据。这一范式转变将全面提升研发效率、降低临床失败率、推动药物开发进入精准、高效且更符合伦理的新时代。

一、传统动物模型的局限性
现代药物研发正面临前所未有的结构性困境。尽管生物医药技术持续高速发展,但候选药物从早期筛选到最终获批上市的成功率依然长期低迷,超过 90% 在临床前研究中表现优异的化合物,进入人体试验后均因疗效不足或安全性问题宣告失败。这一现象的核心根源,在于长期以来药物研发高度依赖动物模型,而小鼠、大鼠、兔、犬乃至非人灵长类动物的生理结构、代谢特征、免疫反应和疾病机制均与人类存在显著差异,无法真实复现人类体内的药物应答、信号通路与毒性响应。
随着治疗模式持续革新,寡核苷酸药物、抗体药物偶联物、靶向蛋白降解剂、细胞治疗等新型疗法不断涌现,这类药物的作用靶点与分子机制往往在动物体内缺乏对应通路,进一步拉大了基础研究与临床应用之间的转化鸿沟。与此同时,传统药物研发流程冗长、成本高昂,平均开发周期超过十年,单药研发成本高达数十亿美元,巨大的投入与极低的成功率形成尖锐矛盾,既制约创新速度,也加剧医疗负担。
在伦理与社会层面,动物实验的争议持续扩大,公众与科研机构对替代、减少和优化动物实验的需求日益强烈。全球监管体系也随之发生历史性转变,美国 FDA 现代化法案 2.0 与 3.0 相继颁布,明确认可新型方法学可以作为动物实验的有效替代或补充;英国发布国家战略加速替代动物实验的技术研发与监管转化;国际组织持续推出指南,支持在药物安全性与有效性评价中优先采用基于人类体系的方法。这些变革共同标志着,以动物实验为核心的传统研发模式已走到转型关口,一场以人为中心的药物研发革命已经到来。
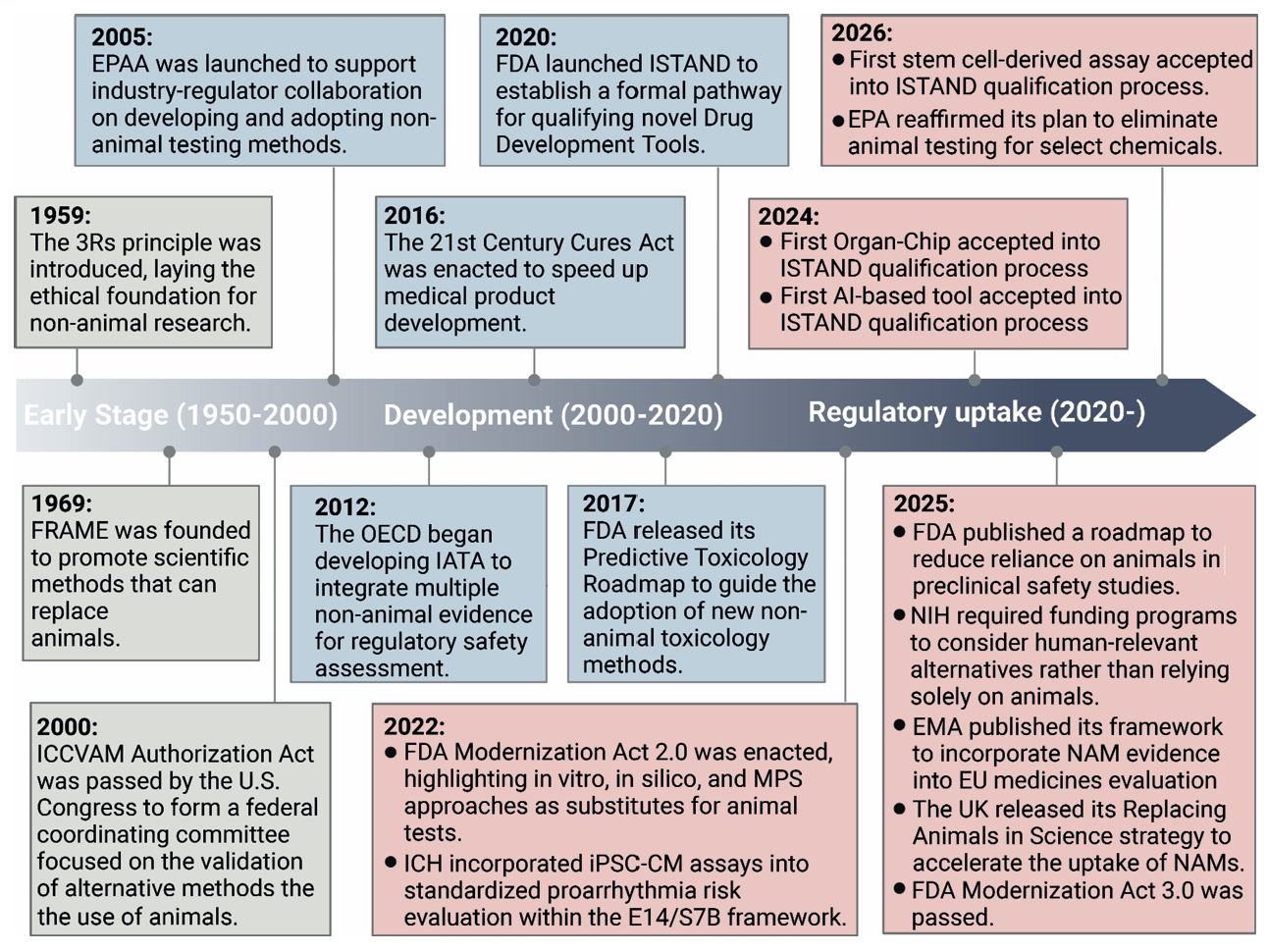
图1 推动以人为中心药物研发的全球监管政策里程碑
二、什么是新方法学(NAMs)?
新型方法学 NAMs 是一套完全围绕人类生物学构建的研发体系,其核心逻辑是放弃对动物模型的依赖,直接使用人类来源的生物材料与计算工具模拟人体生理与病理过程,从而实现更准确、更快速、更经济的药物评价与创新。NAMs 并非单一技术,而是由多层次实验平台与计算工具深度融合形成的完整生态,其最大优势在于从源头消除物种差异带来的预测偏差,让药物研发从 “推测人体反应” 转向 “直接模拟人体反应”。
NAMs 体系具备高度的统一性与协同性,各类平台之间可以数据互通、模型互证,形成从分子、细胞、组织到器官尺度的完整预测链条。与动物模型相比,NAMs 在可控性、重复性、通量与分辨率上均具备显著优势,能够精准揭示药物在人体内的吸收、分布、代谢、排泄与毒性机制,同时支持个体化差异与疾病异质性的定量分析。随着标准化、自动化与数据共享机制不断完善,NAMs 正从概念验证走向大规模应用,逐步成为药物研发的主流支撑体系。
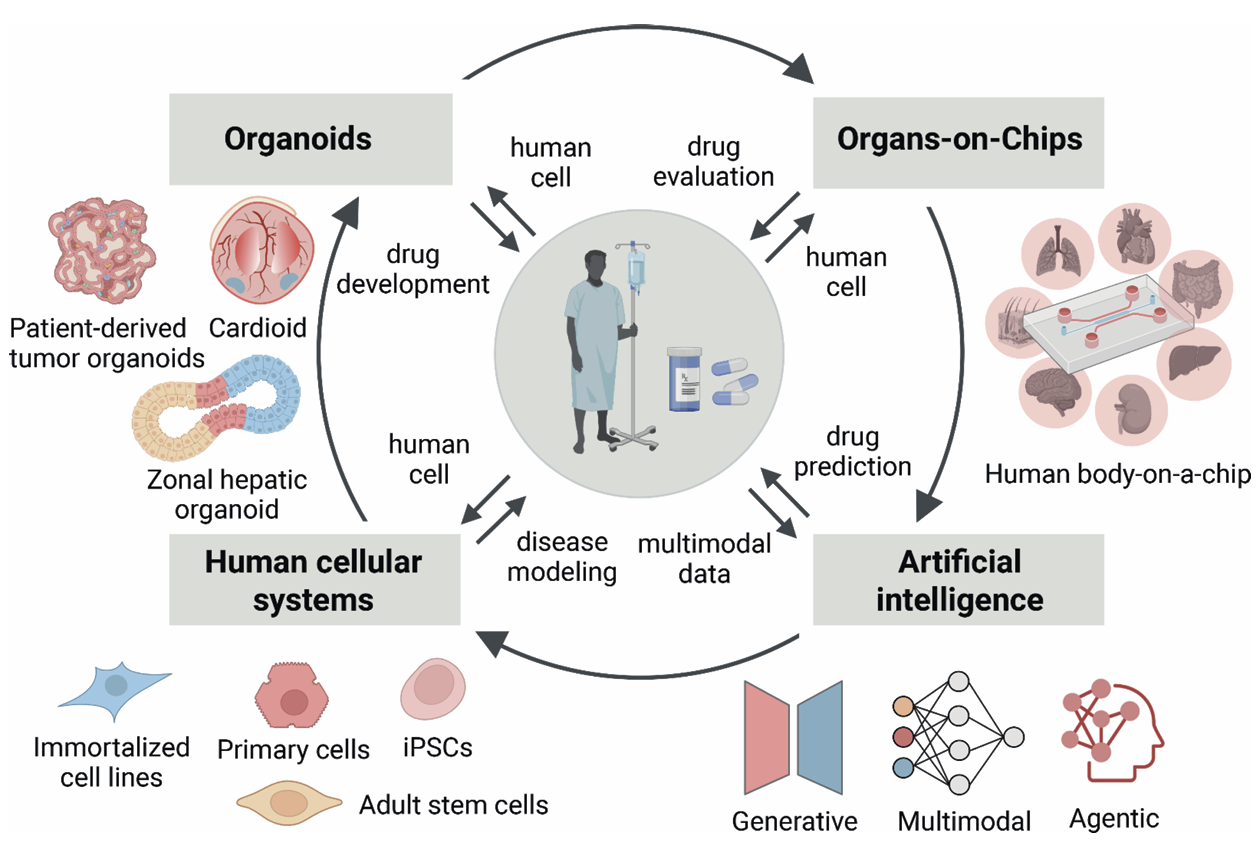
图2 新型方法学(NAMs)融合构建以人为中心的药物研发体系
三、支撑新一代药物研发的三大核心支柱
3.1 人类源细胞模型重建真实生理基础
以人为中心研发的底层基础,是采用人类细胞替代动物细胞,最大程度保留人体组织的真实功能特征。人类原代细胞直接来自人体组织,保留成熟的代谢能力、电生理特性与免疫应答,是评价药物安全性与药效的理想材料,在肝毒性、心脏毒性、肾毒性等关键检测中具备不可替代的价值。永生化细胞系在保证稳定性的同时提升了可扩展性,支持高通量药物筛选与大规模验证,为早期快速筛选提供高效平台。
诱导多能干细胞 iPSC 的出现,进一步突破了细胞来源与伦理限制。iPSC 可由患者的皮肤细胞或血细胞重编程获得,能够无限增殖并定向分化为心肌细胞、肝细胞、神经元、视网膜细胞、胰岛细胞等几乎所有人体细胞类型,为遗传性疾病、罕见病、神经系统疾病与心血管疾病提供了可复制、可遗传、可规模化的疾病模型。患者特异性 iPSC 还能保留个体基因背景,使个体化药物筛选与疗效预测成为可能,为传统模型难以覆盖的疾病领域打开全新空间。
3.2 类器官与器官芯片重构器官功能
二维细胞培养无法还原器官的三维结构、细胞互作与力学微环境,动物模型又存在物种差异,而微生理系统完美解决了这一矛盾,成为 NAMs 体系中最接近人体生理的实验平台。类器官是由干细胞自我组装形成的三维微型器官结构,能够重现器官的关键形态、细胞组成、空间分布与生物学功能,包括脑、心脏、肝脏、肠道、肺、肾脏以及肿瘤类器官。患者来源的肿瘤类器官可高度保留原发肿瘤的基因突变、转录特征与药物敏感性,在肿瘤精准治疗与耐药机制研究中表现出极高的临床预测一致性。
器官芯片则通过微流控技术构建动态生理系统,引入流体剪切力、机械拉伸、血管灌注等物理信号,更真实地模拟呼吸、蠕动、血流等器官活动。肺芯片、肠芯片、血脑屏障芯片、胎盘芯片等相继问世,能够模拟药物跨屏障转运、局部免疫反应、微生物互作等复杂过程。多器官串联芯片可进一步模拟人体多器官协同作用,实现对药物全身代谢与远程毒性的精准预测,其预测能力已在多项研究中超越传统动物实验。
3.3 人工智能与计算模型驱动高效预测与闭环创新
如果说人类细胞与微生理系统是 NAMs 的硬件,人工智能与计算模型就是驱动整个体系高效运转的软件。AI 在药物研发中承担着分子生成、靶点预测、毒性评估、疾病机制解析与临床结果预测的核心功能。生成式 AI 能够直接从蛋白质结构出发,从头设计小分子、多肽、抗体与 PROTAC 分子,突破传统药物化学的设计局限,显著提升先导化合物发现速度与成功率。
多模态大模型能够整合基因组、转录组、蛋白质组、影像数据与临床信息,构建高维度的患者表征模型,实现对药物应答与不良反应的精准预判。数字孪生技术更进一步,将实验数据与生理模型结合,构建个体化虚拟患者,可在计算机中模拟长期疾病进展与药物干预效果,为精准治疗与策略优化提供动态依据。主动学习闭环系统将 AI 预测与实验验证无缝衔接,通过迭代优化持续降低不确定性,使药物开发从试错模式转向理性设计模式。
四、NAMs 重塑从靶点发现到临床转化的药物研发全流程
4.1 实验室闭环加速靶点发现与分子优化
在药物研发早期,NAMs 支持以人类疾病机制为核心的靶点发现与分子设计。AI 模型基于人类蛋白结构与疾病网络筛选潜在靶点,类器官与芯片系统快速验证靶点功能,形成 “计算预测 — 实验验证 — 迭代优化” 的高效闭环。这种模式大幅缩短先导化合物发现周期,降低对大规模化合物库的依赖,同时提高分子在人体中起效的可能性,从源头降低临床失败风险。
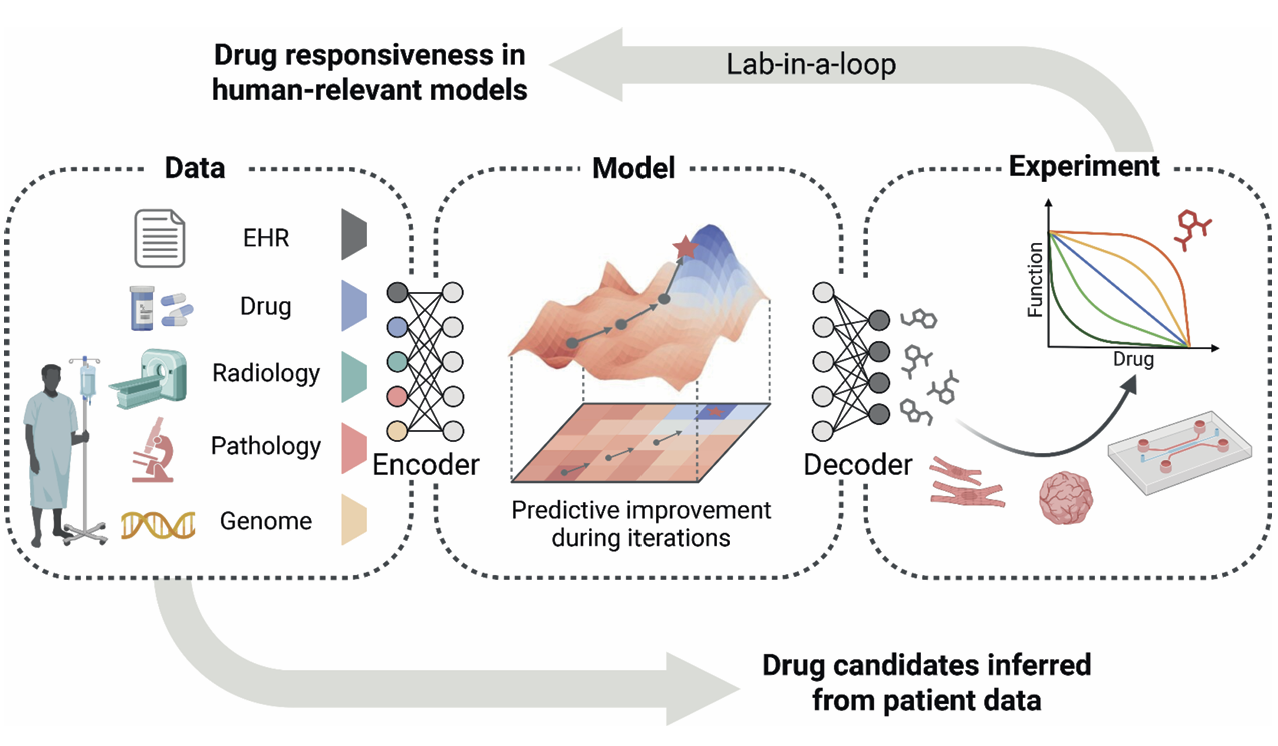
图3 基于人类样本的实验室闭环智能药物研发模式
4.2 器官芯片主导系统性安全性评价
药物毒性是临床失败的主要原因之一,而传统动物实验对人体肝毒性、心脏毒性、肾毒性与神经毒性的预测能力普遍不足。NAMs 体系以人类肝脏芯片、心脏芯片、肾脏芯片为核心,构建高准确度的安全性评价平台,能够捕捉药物在人体中的特异性毒性信号,包括代谢产物毒性、长期累积毒性与个体敏感性毒性。人类肝脏芯片已获得 FDA 监管资格认可,成为替代动物进行肝损伤评价的重要工具,推动安全性评价进入更精准、更可靠的新阶段。
4.3 皿中临床试验实现个体化疗效预测
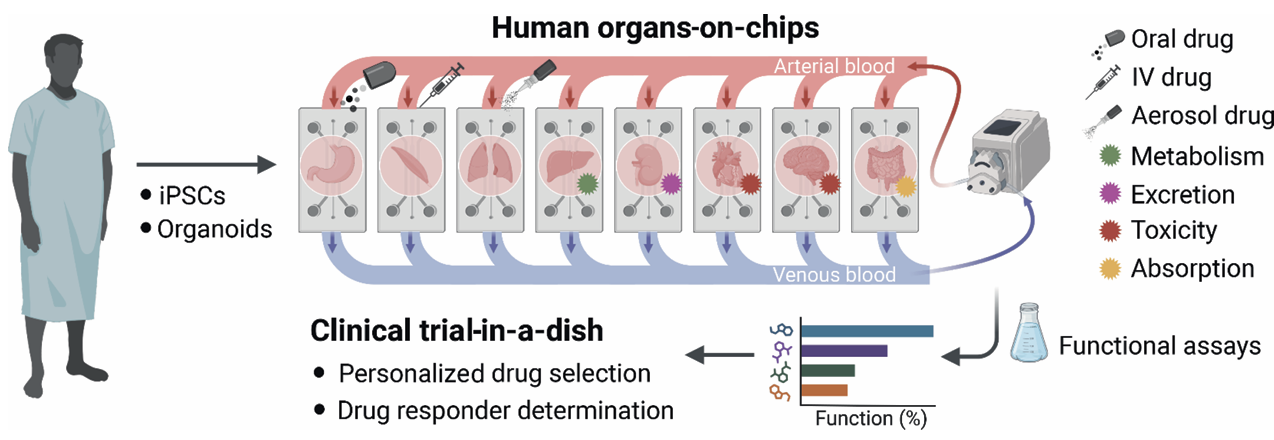
图4 多器官芯片系统与体外 “皿中临床试验” 平台
传统临床试验成本高、周期长、风险大,且难以覆盖个体差异。NAMs 提出 “皿中临床试验” 新模式,利用大规模患者来源类器官或 iPSC 细胞库构建虚拟人群,在体外模拟药物在不同遗传背景、不同疾病亚型中的疗效与毒性,提前筛选优势人群、排除无效患者、预测潜在不良反应。这种模式已在结直肠癌、肺癌、囊性纤维化、心血管疾病等领域得到验证,显著提升临床试验效率,降低研发成本与患者风险。
4.4 数字 — 实验孪生支持长期精准医疗
数字孪生将患者临床数据、多组学信息、器官芯片结果与 AI 模型整合,构建可动态更新的个体化模拟系统,能够持续预测疾病进展、药物疗效与治疗窗口期,为长期疾病管理提供决策支持。在心脏病、肿瘤、神经退行性疾病等慢性疾病中,数字孪生可优化用药方案、评估干预时机、预测复发风险,推动医疗从标准化治疗走向真正的个体化精准医疗。
五、全球监管变革与行业共识为新范式扫清制度障碍
以人为中心的药物研发范式能够快速推进,离不开全球监管体系的同步革新。美国、欧盟、英国、日本等主要医药监管机构相继发布政策,明确支持 NAMs 替代动物实验,并建立标准化验证与认可通道。FDA 推出 ISTAND 计划,专门对器官芯片、AI 模型等新型技术进行资格认定;OECD 发布体外方法良好实践规范,推动全球技术标准统一;多国法规明确允许在新药申报中使用体外数据与计算模型替代动物实验数据。
监管变革的核心逻辑,是认可基于人类体系的预测结果比动物实验更具临床相关性。随着越来越多的 NAMs 平台获得监管认可,行业内部也形成共识,大型制药企业纷纷建立以类器官、器官芯片和 AI 为核心的研发平台,将新型方法学纳入核心管线。学术界、工业界与监管机构的协同推进,使以人为中心的研发范式从前沿探索转变为行业标准。
六、总结与展望
传统依赖动物实验的药物研发模式,受限于物种差异、效率低下、成本高昂与伦理压力,已难以支撑现代生物医药的创新需求。以 NAMs 为核心的以人为中心新范式,通过人类源细胞模型、类器官、器官芯片与人工智能计算模型的深度融合,构建了更贴近人体真实生理的药物研发体系,显著提升预测准确性、缩短研发周期、降低成本,并推动药物研究走向精准化与个体化。
未来药研多步相关的动物实验验证将逐步取消,而是以人源细胞系构建的类器官、器官芯片和计算模型的结果为重要依据。随着技术不断成熟、标准持续统一、数据生态日益完善,NAMs 将全面渗透靶点发现、分子设计、安全性评价、临床预测与精准医疗等全链条环节,彻底重构药物研发的底层逻辑。这场革命不仅是科学与技术的突破,更是生物医药行业走向更高效、更可靠、更符合伦理的历史性跨越,将为全球患者带来更快、更安全、更精准的创新疗法。
论文链接:https://www.science.org/doi/10.1126/science.aeb0045 | 


























