分子胶(MGs)通过调节蛋白质相互作用来抑制、激活或降解靶点。传统分子胶,如thalidomide(沙利度胺)、cyclosporin(环孢菌素)和fusicoccin(一种真菌化脓毒素)等是偶然发现的,但开发分子胶的理性设计方法仍具有挑战。分子胶结构活性关系(SAR)知识的最新进展促成了新型分子胶的理性设计。此外,基于结构的新设计技术增加了临床前分子胶的靶点多样性,多个候选药物已进入临床试验。
近日,美国康涅狄格大学团队在Trends in Pharmacological Sciences(IF = 19.9)期刊发表了一篇题为“Molecular glues evolve from serendipity to rational design”的综述,本篇综述重点介绍了分子胶从天然产物到合成化合物的发展历程,并讨论了新兴技术的整合,以指导分子胶理性设计成为新的治疗剂。

研究内容
1. 以天然靶向为引领,攻克不可成药靶点
蛋白质-蛋白质相互作用(PPIs)对于细胞功能(如信号转导和基因表达)至关重要,可作为治疗人类疾病的潜在重要靶点。包含大、平或动态界面且缺乏深口袋的PPIs难以通过小分子抑制剂进行靶向。许多与疾病相关的参与PPIs的蛋白质,如IKZF1和KRAS,无法通过传统药物发现方法进行靶向,因此被称为“不可成药”靶点,这给新抑制剂的开发带来了重大挑战。
与抑制剂不同,分子胶通过增强相关蛋白质之间的亲和力来形成三元蛋白质复合物。其作用是对信号传导事件起到抑制或促进作用,或者稳定或降低蛋白质表达。天然产物通常具有形成三元复合物的优势,然而它们必须是小分子才能被视为分子胶。免疫反应系统提供了大量实例(图 1):①泛素-蛋白酶体降解途径是免疫反应中的关键角色,它降解外来蛋白质并生成肽抗原。分子胶可以将其靶向作用于难以成药的蛋白质;②先天免疫中的分子胶。Toll样受体(TLRs)和NOD样受体(NLRs)在与外来DNA分子结合时形成三元复合物,从而激活免疫系统;③T细胞受体的分子胶。虽然肽抗原会触发MHC和TCR的复合物,但免疫学的最新发现表明,非典型抗原可作为常规或共价分子胶。这些例子表明,MGs能够超越典型的PPIs,从而调节免疫识别和药物过敏反应。
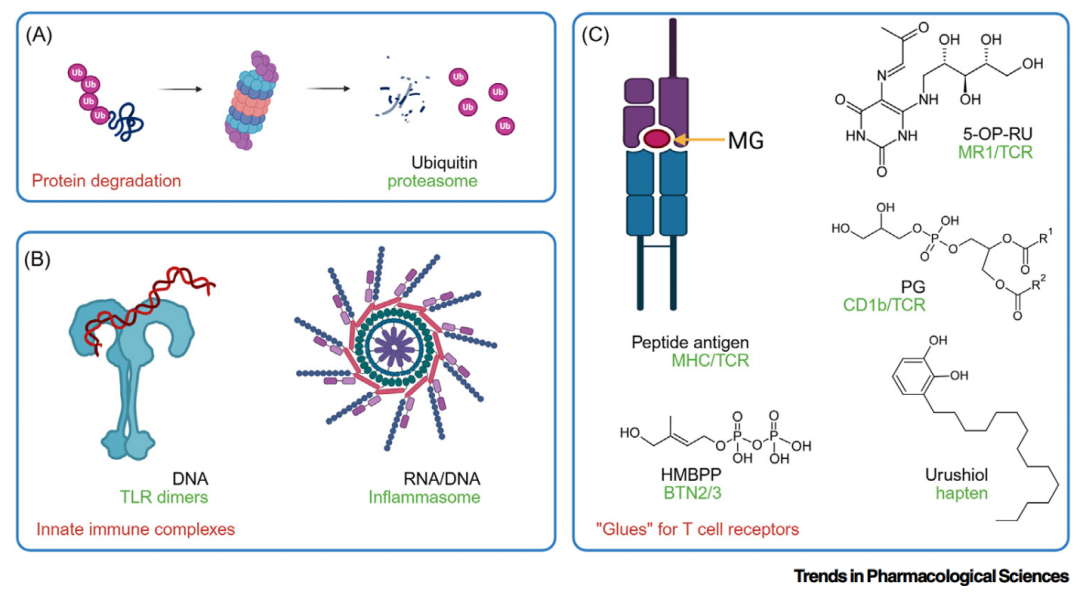
图1 免疫作为分子胶的来源
2. 作为抑制剂、激活剂、稳定剂和降解剂的MGs的开发
分子胶的发展历程如图2所示,过去几年中,可用的分子胶数量不断增加;分子胶在化学结构上多种多样,包括天然产物和有机合成两大类别,其大小从约175 Da~1200 Da不等。分子胶的发现和优化如今已成为现代药物研发中的关键领域,同时结构是决定分子胶能否有效发挥蛋白质-蛋白质相互作用调节剂的关键。
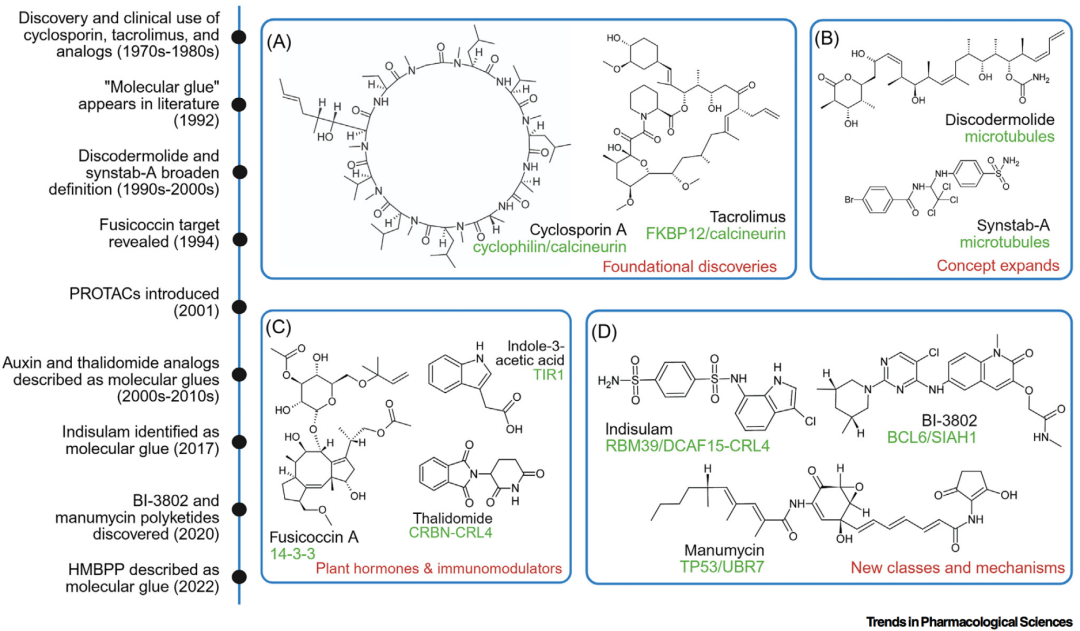
图2 分子胶发现的主要里程碑时间线
2.1 合成性分子胶
可合成分子胶的发现途径通常遵循两种主要策略之一:①先展示策略,即优化化学物质以招募特定目标蛋白;②先目标策略,即针对期望的目标进行筛选,从而揭示诱导新三元复合物的小分子。过去,大多数合成分子胶水都是通过先展示策略发现的。无论哪种情况,都会在初始命中之后进行优化,再通过结构和药理学分析来提高效力和选择性。
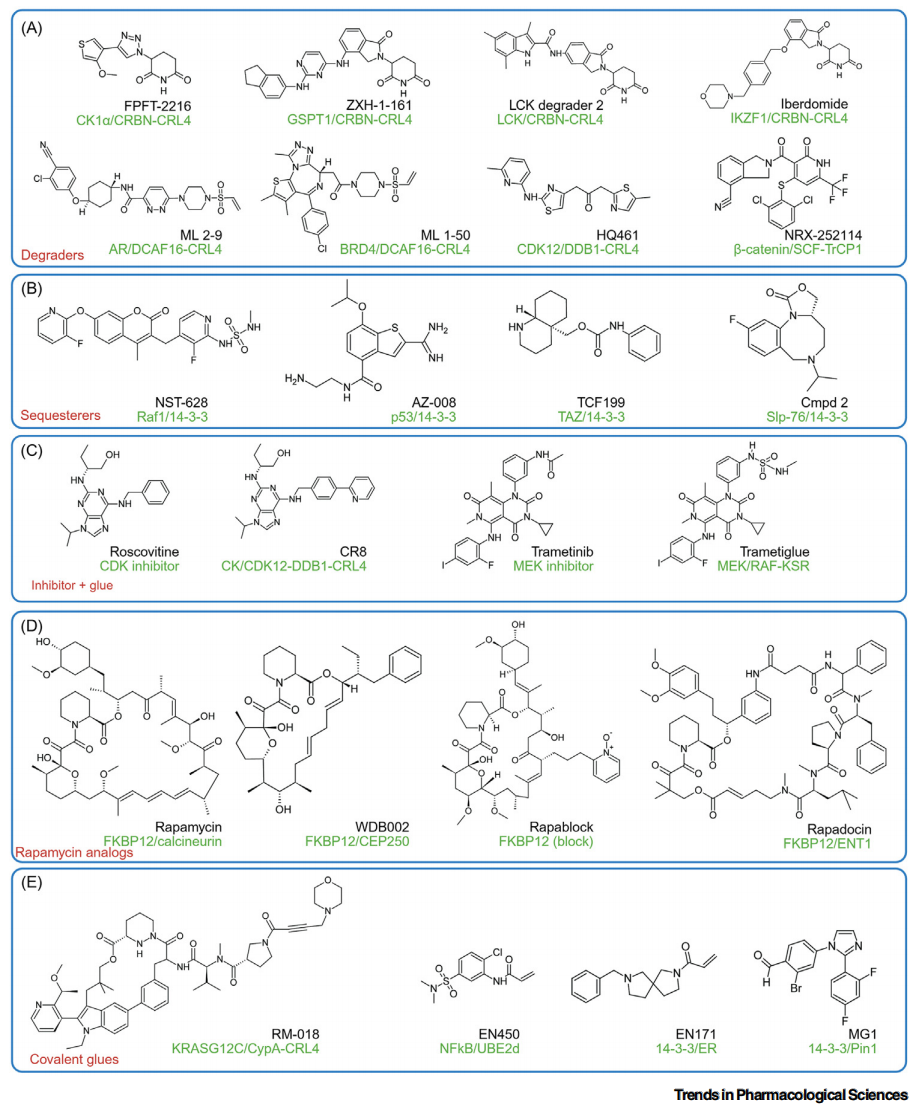
图3 合成分子胶
(A)降解型分子胶的示例;(B)利用14-3-3作为展示蛋白的非降解型分子胶示例;(C)由抑制剂衍生的分子胶;(D)由天然产物如rapamycin和WDB002衍生的分子胶;(E)共价分子胶
2.2 分子胶的作用机制:从结合模式到生物学效应
分子胶的作用机制如图4所示,临床上使用的分子胶可根据其作用机制而非结构或结合特性分为三类。
Ⅰ类分子胶通过诱导蛋白质-蛋白质相互作用来物理阻断或“屏蔽”目标蛋白的功能界面,从而抑制其天然相互作用。这类分子胶在免疫抑制和癌症治疗中具有特别的应用价值。cyclophilin和tacrolimus就是其中的典型代表,前者与亲环素结合,后者与FKBP12结合,两者均能与钙调神经磷酸酶形成复合物,从而抑制信号传导。
II型分子胶与蛋白质-蛋白质相互作用结合,并改变其构象状态,从而抑制或稳定特定的蛋白质功能。这种机制对于蛋白质聚集或动态信号传导相关疾病(如淀粉样变性或癌症)具有重要价值。此类包括肽、小分子抗原以及微管稳定剂。
III型分子胶类药物诱导蛋白质-蛋白质相互作用,通过招募到诸如CRBN、VHL、DCAF15或DDB1等E3泛素连接酶,从而导致目标蛋白的降解,这一过程涉及泛素化和蛋白酶体降解。E3连接酶通过诱导邻近作用介导分子胶的作用机制,即分子胶在一种蛋白质上创造或重塑一个新表位,以招募另一种蛋白质形成三元复合物。在降解过程中,这将目标蛋白质带到E3连接酶附近,从而使其能够通过泛素-蛋白酶体系统进行降解。
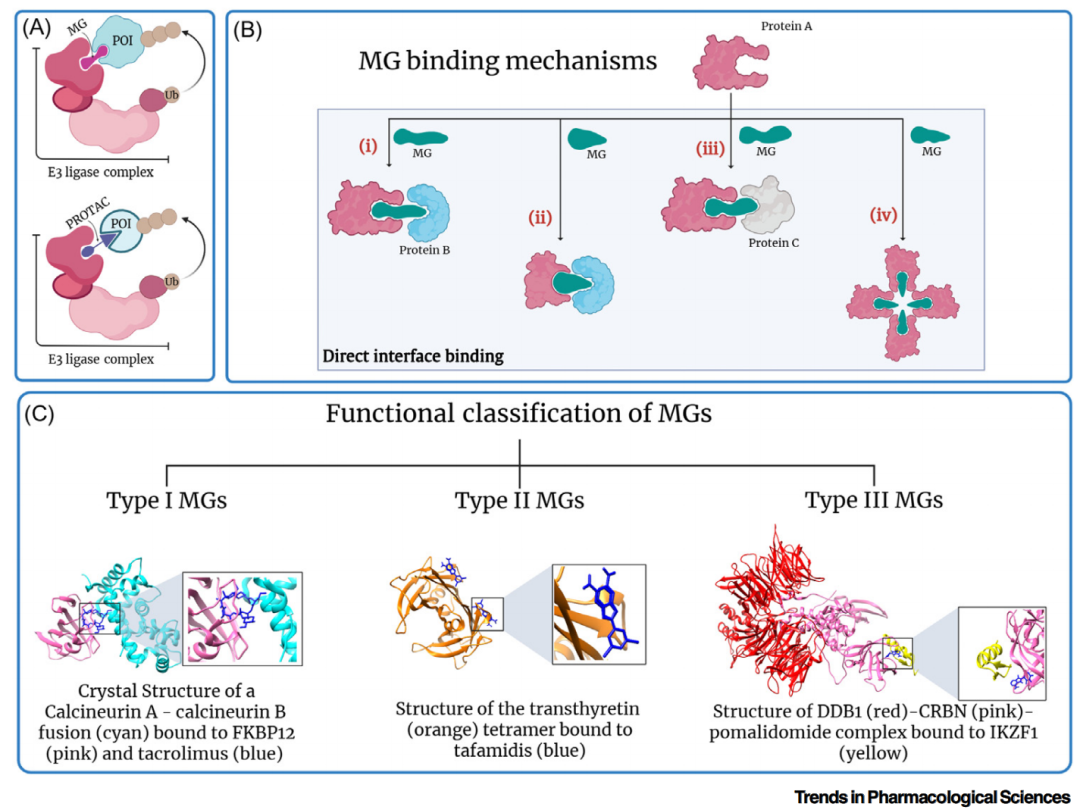
图4 分子胶的机制分类
(A)分子胶与蛋白水解靶向嵌合体(PROTACs)机制的差异。分子胶是单价化合物,可与两种蛋白质形成三元复合物,而PROTACs是双价化合物,可将两种蛋白质连接在一起。(B)分子胶的主要作用机制:(i)增强和稳定蛋白质相互作用,(ii)修复因突变而减弱的蛋白质相互作用,(iii)诱导新的蛋白质相互作用,(iv)自缔合。(C)分子胶的功能分类:(I)阻断天然相互作用,(II)稳定天然相互作用,(III)降解
3. 推动下一代分子胶发现的技术
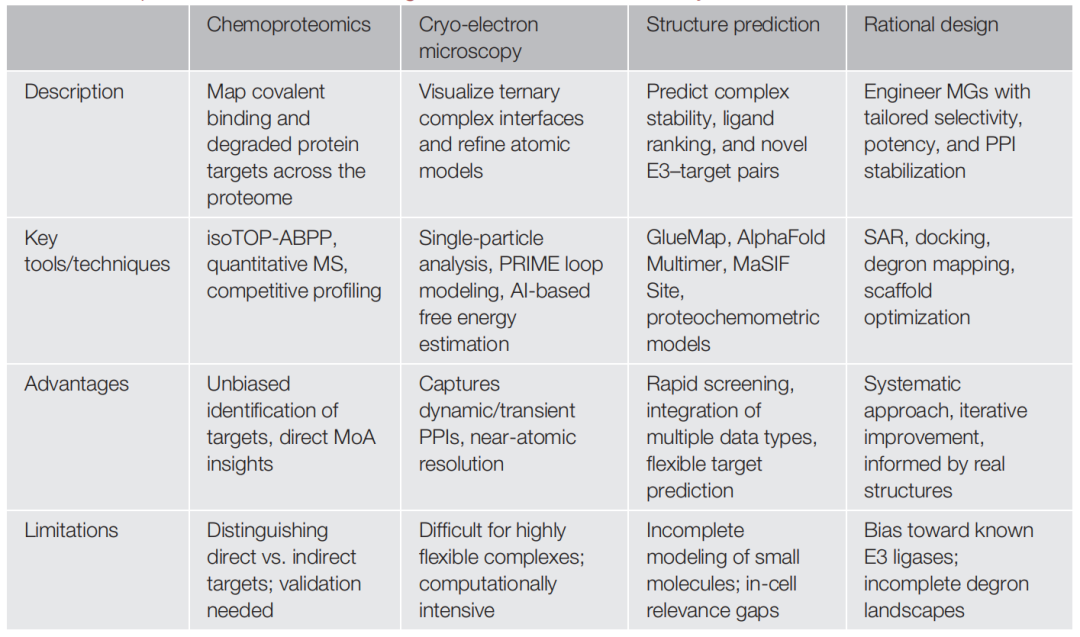
(i)化学设计和构效关系(SAR)确定,通过有针对性地修改化学基团来调整选择性和效力(例如,改变CRBN调节剂或添加共价手柄);
(ii)通过晶体学或冷冻电镜获得的高分辨率三元复合物结构(例如,靶点、E3连接酶、胶水)所提供的结构/机制见解,通常借助人工智能(AI)增强,以识别降解子基序或界面口袋;
(iii)计算和机器学习方法——例如对接、虚拟筛选和基于AI的表面评分——以预测有利的界面并排列候选物;
(iv)通过化学蛋白质组学、生物物理测定和细胞降解研究进行迭代验证,以优化设计。
表1 分子胶发现中技术发展的比较
4. 转化和临床进展
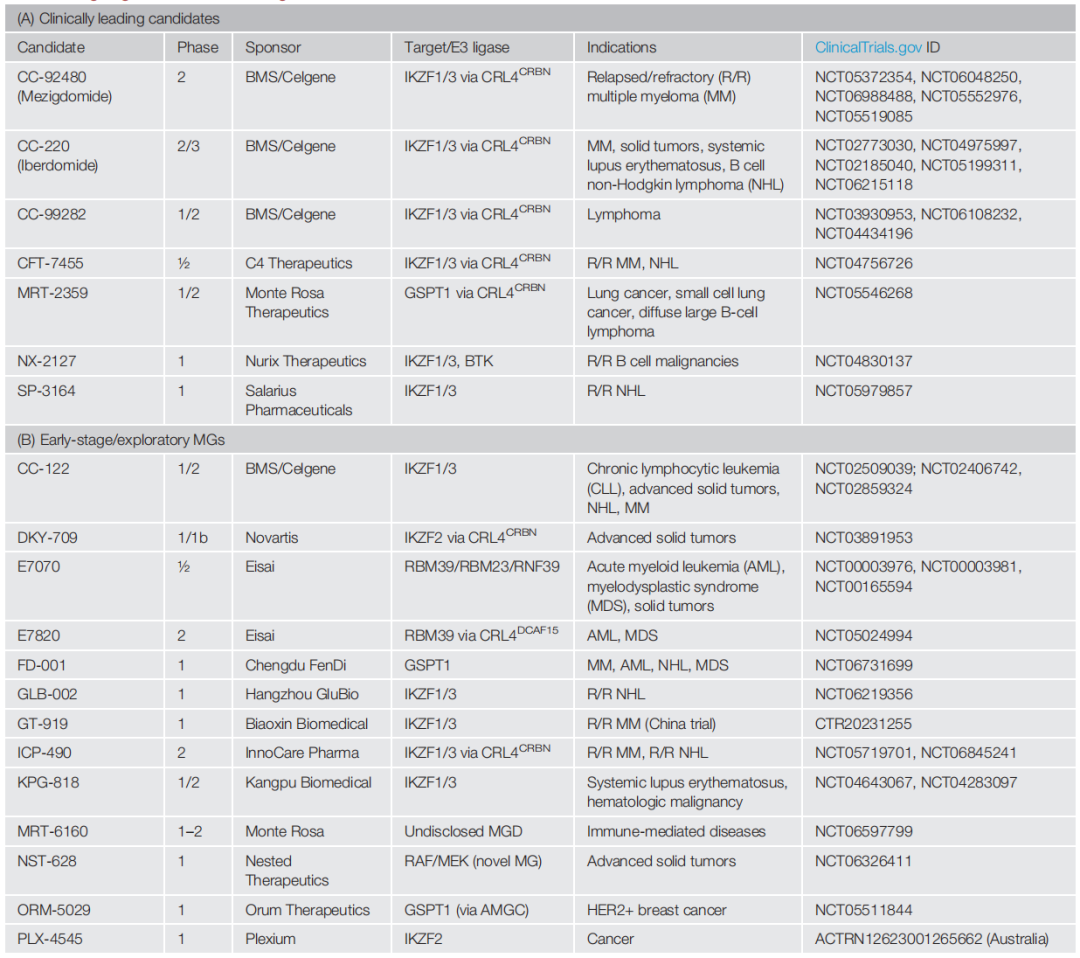
该领域正从概念验证向广泛的临床应用过渡,有几种药物有望重塑癌症和免疫介导性疾病的治疗模式。表2总结了从ClinicalTrials.gov和中国临床试验注册中心收集的正在进行的临床试验的全面概览,其中区分了处于临床领先地位的候选药物(A)和处于早期阶段或探索性的MG(B)。
表2 分子胶正在进行的临床试验
总结
(1)分子胶通过调节蛋白质-蛋白质相互作用,将此前难以成药的蛋白质作为靶点进行抑制、稳定或降解;
(2)天然产物启发了合成分子胶的开发,如今化学家们正在扩大这些化合物的多样性和临床应用价值;
(3)MGs在三元复合物的形成中表现出机制多样性,通过直接界面结合和诱导邻近作用实现;
(4)诸如冷冻电镜、人工智能驱动建模和化学蛋白质组学等技术正在加速膜蛋白的发现和合理设计;
(5)关键突破包括与CRBN结合的分子胶,这使得靶向蛋白降解成为可能,并引发了一波临床试验热潮。
参考文献
Shrivastav P, Singh R, Wiemer AJ. Molecular glues evolve from serendipity to rational design. Trends in Pharmacological Sciences. 2026, 47(1): 85-99.
文章改编转载自微信公众号:智药邦
原文链接:https://mp.weixin.qq.com/s/q_uQJhAw-B7k9ViOyNdujw | 


























