本帖最后由 哈奇一 于 2026-2-27 14:41 编辑
国际团队在《Nature Biotechnology》2025 年 43 卷发表该研究,提出量子 - 经典混合生成模型研发 KRAS 抑制剂。模型基于 16 量子比特,通过量子 Born 规则等核心公式建模,从 110 万条数据中生成分子,合成 15 种候选物。其中 ISM061-018-2 对 KRAS-G12D 的结合亲和力达 1.4μM,泛 Ras 活性显著且无明显毒性;ISM061-022 具突变体选择性。量子模型使分子通过筛选的比例提升 21.5%,为 KRAS 靶向治疗提供新路径。

KRAS 基因突变被称为 “癌症之王”,是肺癌、胰腺癌等多种恶性肿瘤的核心驱动因素,长期以来因靶点结构复杂,一直是药物研发的 “硬骨头”。传统药物发现周期长达十年、成本高昂,且难以突破化学空间的探索瓶颈。国际团队在《Nature Biotechnology》发表突破性研究,提出量子 - 经典混合生成模型,成功设计并合成 15 种潜在 KRAS 抑制剂,其中 2 种展现出明确药用潜力,为攻克这一 “不可成药” 靶点提供了全新路径。
一、KRAS 抑制剂研发的 “双重困境”
KRAS 蛋白的特殊性让药物研发面临前所未有的挑战:
靶点结构难靶向:KRAS 蛋白表面光滑、结合口袋不明显,传统小分子药物难以精准结合;且突变类型多样(G12D、G12C、G12R 等),单一抑制剂难以覆盖多种突变;
化学空间太庞大:潜在药物分子的化学空间规模高达1060,传统虚拟筛选和实验试错难以高效找到有效分子;
研发效率低下:从靶点验证到候选药物筛选,传统流程需耗费大量时间和资源,成功率不足 10%,KRAS 靶点的研发更是屡遭挫败。
这些困境让 KRAS 抑制剂的研发长期停滞,临床需求迫切待解。
二、量子 - 经典混合模型:精准探索药物化学空间
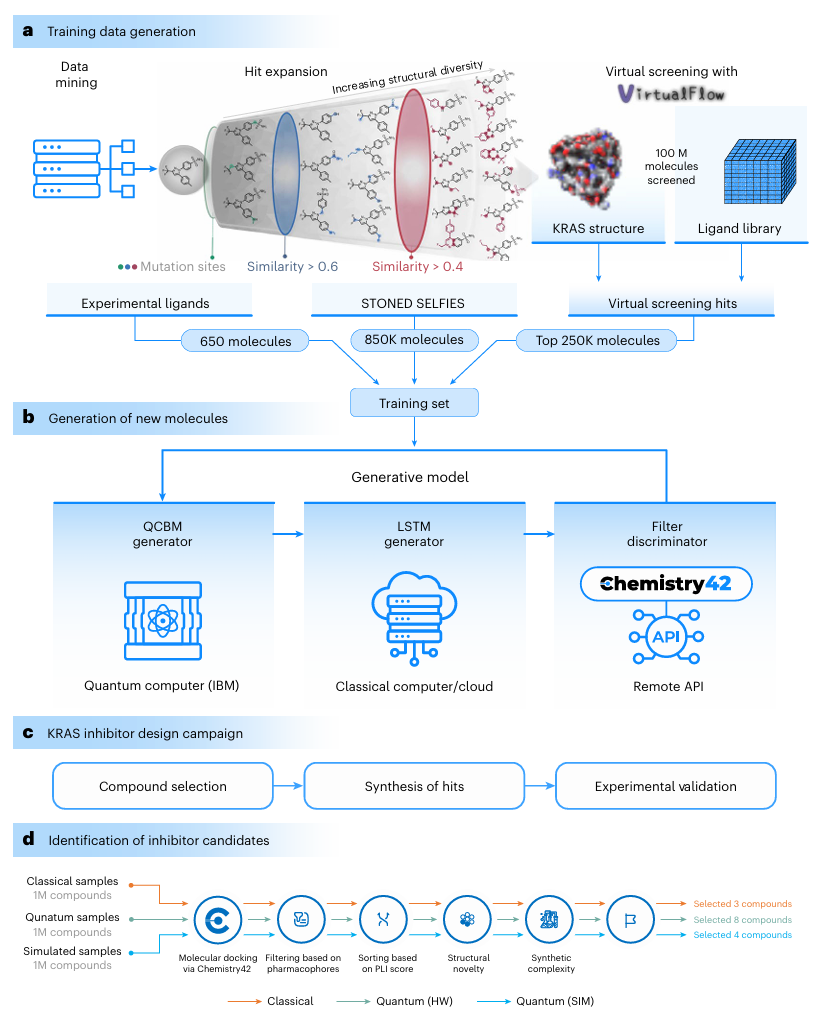
KRAS 抑制剂研发的混合量子 - 经典框架流程图
研究团队创新性地将量子计算的并行优势与经典 AI 的序列学习能力结合,构建三级研发流程,高效突破 KRAS 药物研发瓶颈:
2.1 第一步:构建超百万级训练数据集
基础数据:从文献中筛选 650 种经实验验证的 KRAS 抑制剂,作为核心训练样本;
数据扩充:通过 STONED-SELFIES 算法生成 850,000 种结构相似的衍生物,同时利用 VirtualFlow 2.0 平台虚拟筛选 1 亿个分子,筛选出 250,000 个高潜力候选者;
最终数据集:整合后形成含 110 万条数据的高质量训练集,覆盖 KRAS 靶点的关键结合特征。
2.2 第二步:量子 - 经典混合生成模型
模型由 “量子生成器 + 经典生成器 + AI 验证器” 三部分组成,协同发挥优势:
量子电路玻恩机(QCBM):基于 16 量子比特的 IBM 量子处理器,利用量子叠加和纠缠特性,高效探索复杂化学空间的概率分布,生成具有新颖结构的分子骨架。其核心是通过量子态测量概率建模分子分布,遵循量子力学 Born 规则:
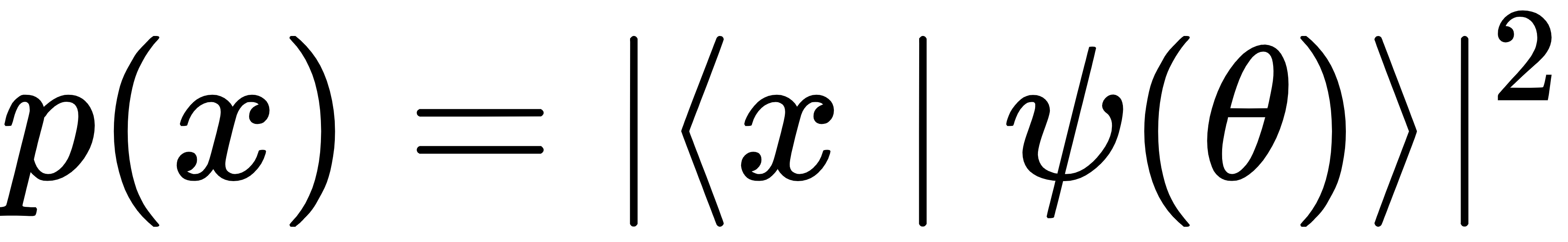
其中|ψ(θ)⟩是参数化量子态,θ为量子电路参数,x为分子的量子编码表示,该公式确保生成分子的概率分布符合量子力学规律,能高效覆盖复杂化学空间;
长短期记忆网络(LSTM):作为经典生成器,学习分子序列规律(以 SELFIES 分子编码形式输入),对量子生成的骨架进行结构优化,确保分子的合成可行性。其细胞状态更新核心公式为:
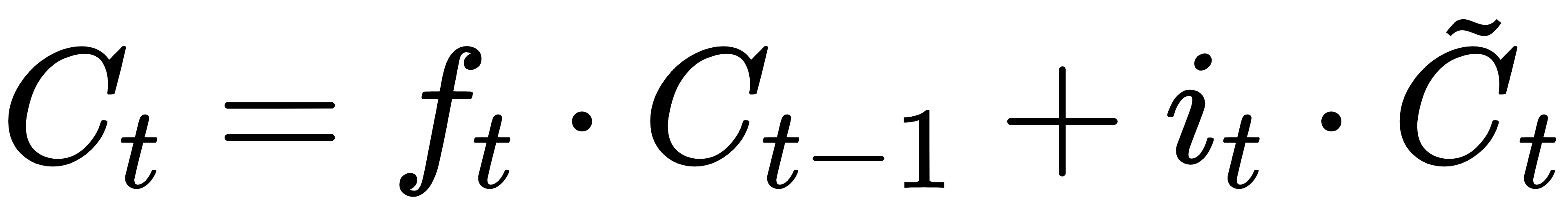
其中ft为遗忘门、it为输入门、C~t为候选细胞状态,通过该机制捕捉分子序列的长程依赖关系,优化分子结构的合理性;
Chemistry42 验证器:作为奖励函数,实时评估生成分子的结合亲和力(PLI 评分)、合成可达性等关键属性,反馈指导模型迭代优化。奖励函数经 softmax 归一化后为:

其中R(x)为分子的综合评分(含结合活性、合成性等),确保模型优先生成高潜力药物分子。
核心创新在于量子与经典的协同:量子模型突破经典算法的探索局限,经典模型保障分子的实用性,验证器则精准把控药物属性,形成 “生成 - 优化 - 验证” 的闭环。
2.3 第三步:实验验证与筛选
从模型生成的 100 万个分子中,通过 docking 评分、药代动力学筛选,最终选择 15 个候选分子进行化学合成,再通过表面等离子体共振(SPR)和细胞实验验证活性。
三、突破性成果:2 种候选药物展现强潜力
实验验证结果令人振奋,核心成果如下:
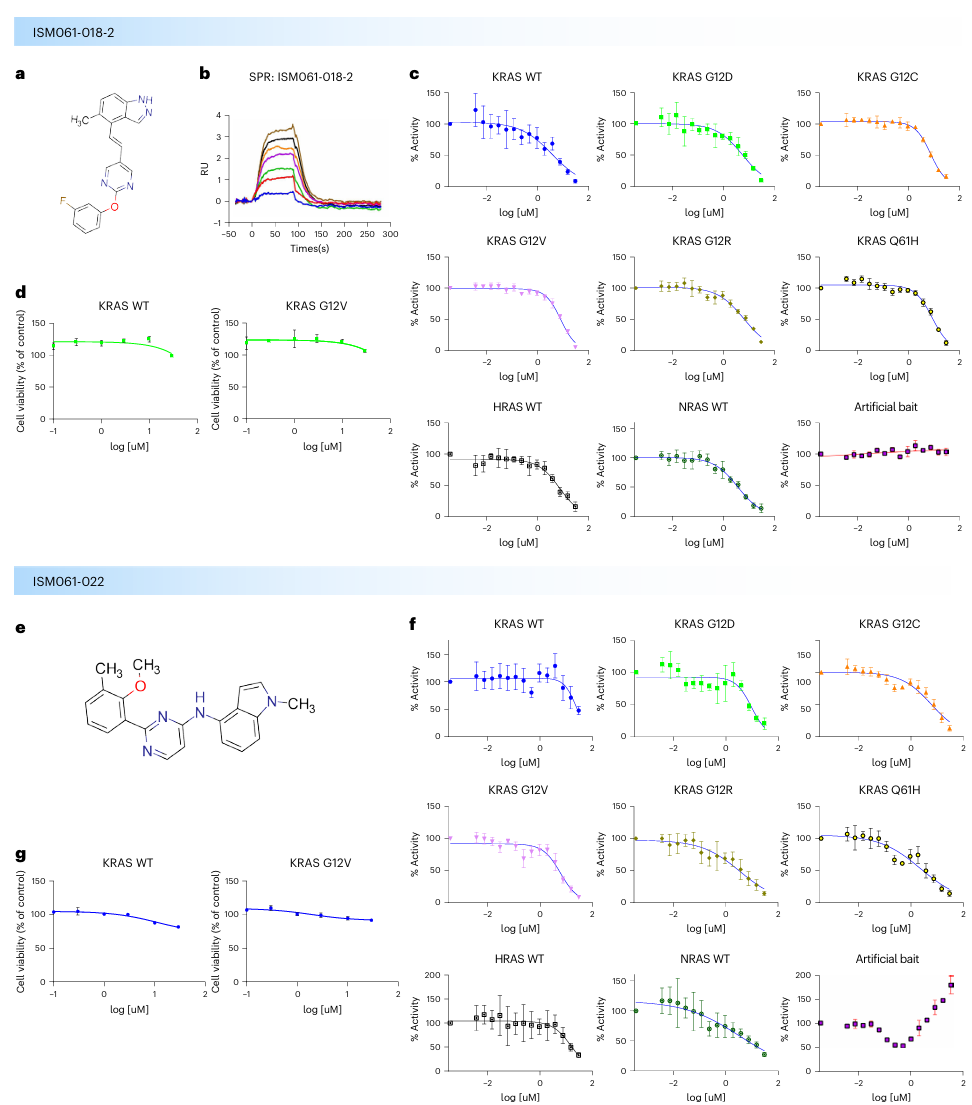
候选化合物 ISM061-018-2 与 ISM061-022 的活性与细胞毒性验证图
ISM061-018-2:对 KRAS-G12D 突变体的结合亲和力达 1.4μM,且具有泛 Ras 活性 —— 能有效抑制 KRAS 野生型及 G12V、G12R 等多种突变体与 Raf1 的相互作用,IC50值处于微摩尔级;无明显细胞毒性,30μM 浓度下对 HEK293 细胞活力无显著影响;NMR 实验证实其结合于 KRAS 的 switch II 口袋,作用机制明确。
ISM061-022:展现出突变体选择性,对 KRAS-G12R 和 Q61H 突变体抑制效果显著,同样无严重细胞毒性,为针对性治疗特定 KRAS 突变癌症提供可能。
模型优势:量子 - 经典混合模型生成的分子,通过合成性和稳定性筛选的比例较纯经典 LSTM 模型提升 21.5%,且分子结构新颖性更高,拓展了 KRAS 抑制剂的化学空间。
四、技术价值:重塑药物研发范式
该研究的突破不仅在于找到潜在 KRAS 抑制剂,更在于建立了量子计算辅助药物发现的高效范式:
大幅缩短研发周期:将传统数年的候选药物筛选过程缩短至数月,显著降低时间成本;
拓展化学空间探索:量子计算的并行特性让模型能探索经典算法难以触及的分子结构,提升新药发现概率;
普适性强:该框架可迁移至其他 “不可成药” 靶点(如 TP53、MYC),为抗癌药物研发提供通用工具。
五、总结:量子计算开启抗癌新药研发新时代
量子 - 经典混合生成模型以 16 量子比特为核心,通过 Born 规则、LSTM 细胞状态更新等关键公式构建高效生成机制,成功突破 KRAS 抑制剂研发的长期困境,生成的 2 种候选药物展现出明确的结合活性和低毒性,为癌症治疗带来新希望。这一成果证明,量子计算与 AI 的融合不仅是技术探索,更已进入实际应用阶段,有望彻底改变药物研发的底层逻辑。
未来,随着量子硬件的升级(更多量子比特、更高门保真度)和模型的持续优化,量子计算将在更多疾病靶点的药物研发中发挥核心作用,让 “精准抗癌” 从愿景走向现实。
原文链接:https://www.nature.com/articles/s41587-024-02526-3 | 


























